基礎研究について Basic Research
心不全
心不全基礎研究グループについて
心不全の病態進展の機序は、血行動態や心臓の形態・機能、組織学的変化のみではとらえることができず、細胞機能、遺伝子・タンパク機能の変化が中心的な役割をになっています。心不全基礎研究グループでは,松島、橋本、池田が指導教官として心不全における心機能障害の進展機序解明と新規治療法開発を目標として,分子レベルでの解明を目指し,既存の概念にとらわれない自由な発想で研究を行っています.また,基礎研究の知見をもとにした臨床研究およびリアルワールドデータを用いた臨床研究への展開も進めています.日常診療に根差したクリニカルクエスチョンを解決し,世界に発信できるエビデンスを構築することを目指しています。

心不全におけるレドックス制御と
その意義に関する研究
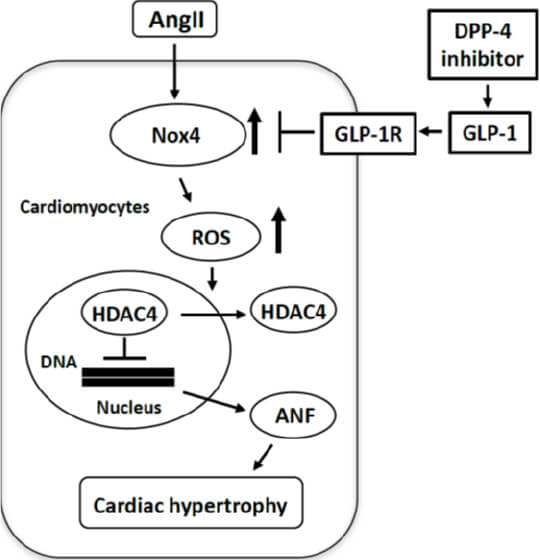
活性酸素種(ROS)に関する研究に取り組み、ミトコンドリア(mt)特異的抗酸化酵素によるROS消去が心不全を改善することを初めて明らかにしました(Circulation. 2006)。 さらにNADPHoxidase4(Nox4)が不全心の主要なROSの産生源であり(PNAS. 2010)、Nox4による核内HDAC4の酸化修飾が心肥大を促進することを報告しました(Circ Res. 2013)。また、ROSは増加だけでなく極度に抑制されても心筋障害を引き起こすことを見出し(Circ Res. 2013)、Nox4C末端566番目のチロシンのリン酸化による翻訳後修飾がNox4を負に制御するという新たな活性制御機序を解明することで(JClin Invest.2016)、ROSの質および量的なレッドクス制御の重要性を明らかにしましたNox4制御の臨床応用を目指して研究を進め、DPP4-GLP1系が心臓におけるNox4を抑制することで心肥大を軽減することを明らかにし(Hypertension.2020)、こられの知見をもとに臨床研究を行い、DPP-4阻害薬が心肥大を含むHFpEF患者において良好な予後と関連することを初めて報告しました(JACC Asia 2023)。
心筋炎症の新規制御機序に関する研究
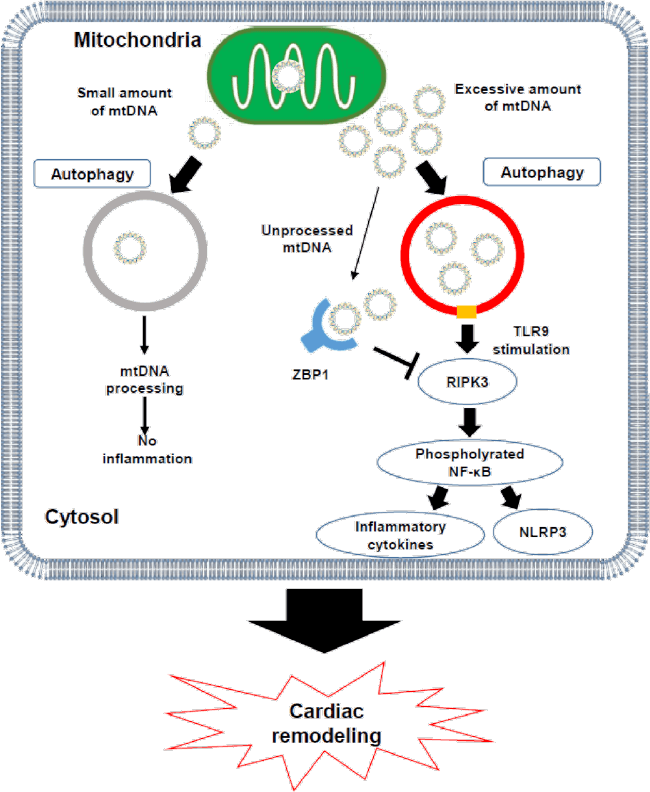
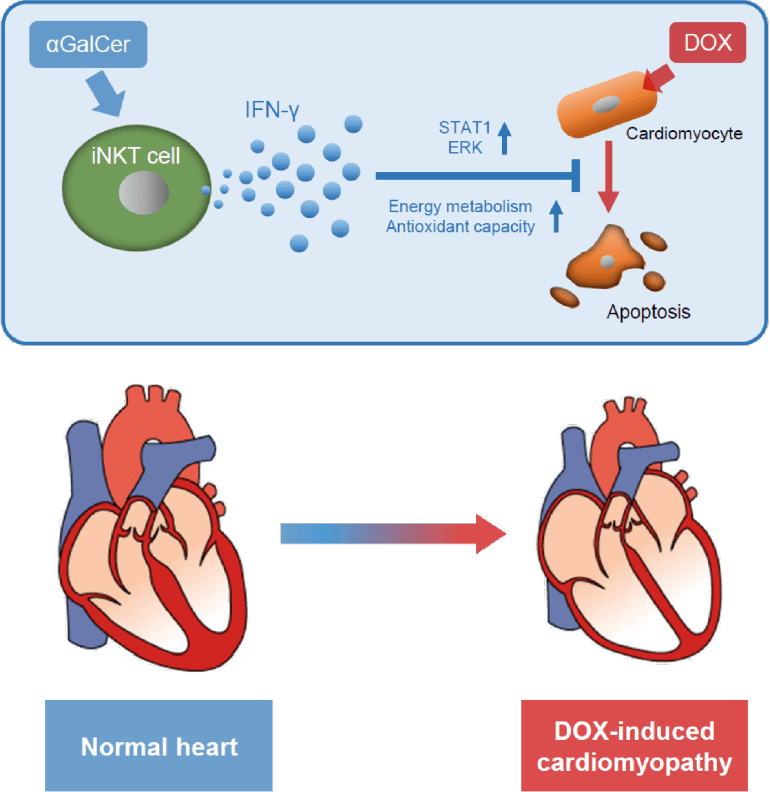
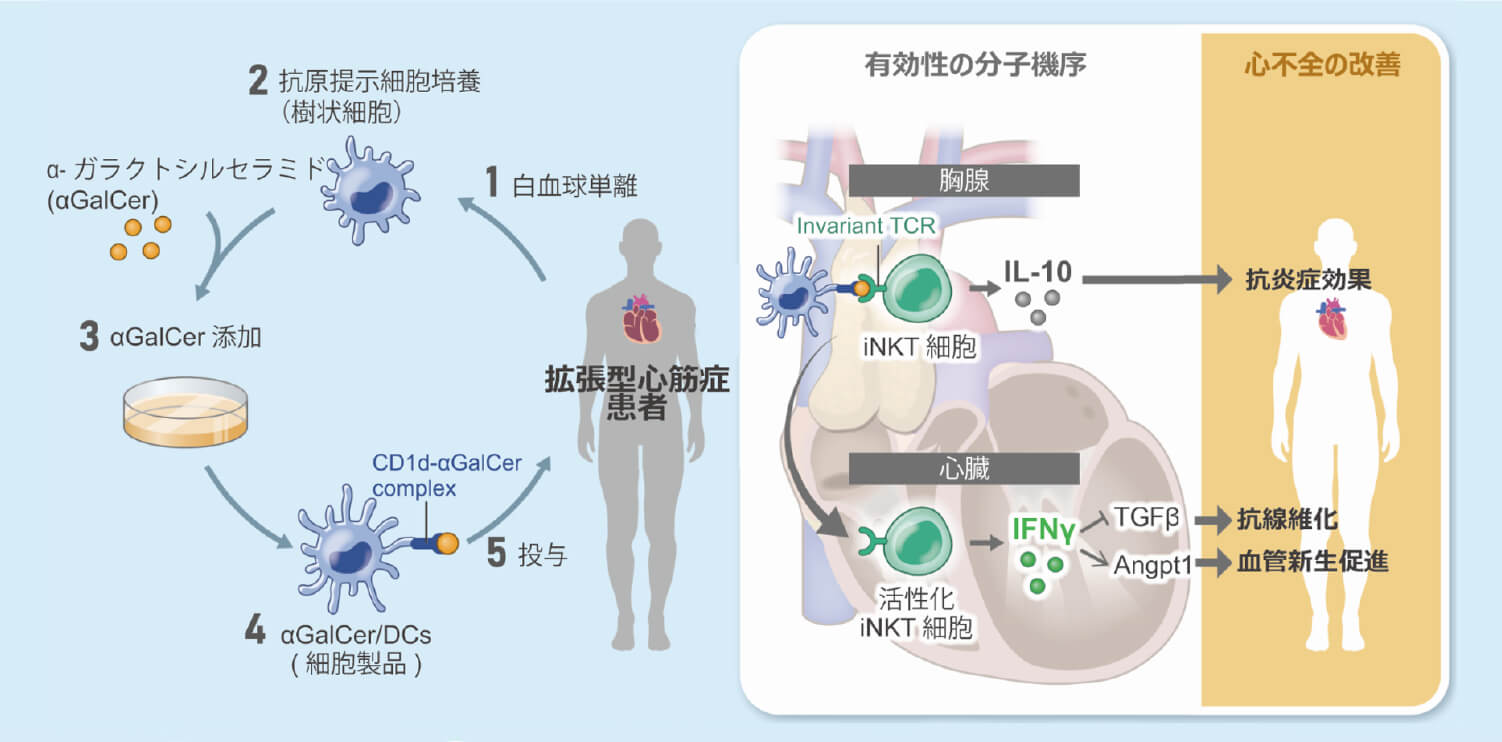
心筋炎症における新規治療標的の創出に関する研究も進めてきました。ROSによりmtDNAが障害されますが、mtDNAが細胞質へ漏出することでインフラマソームを介してIL-6が上昇し心筋炎症が惹起され、ZBP1はそのmtDNAを捕捉することで抗炎症作用を果たす重要な内因性保護因子であることを明かにしました(Circ Res. 2023)。また、炎症を調整するユニークな特徴を有するNKT細胞がIFN-γを介して細胞内シグナルのERKなどを活性化することで心保護的に作用することを見出しました(Circ HF. 2022, JACC BTS. 2023)。これらの成果をもとに、ヒトにおけるNKT細胞の心不全への有効性に関する医師主導治験を進めております。
心筋リモデリングの進展機序解明および細胞連関・臓器連関に関する研究
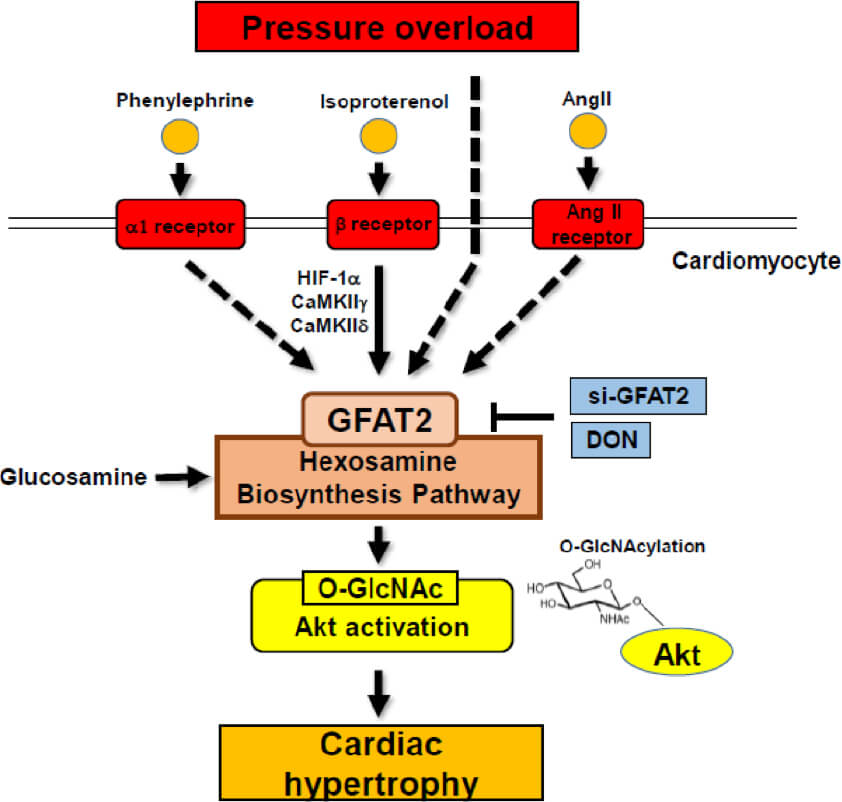
糖代謝の副経路であるヘキソサミン合成経路によるO-GlcNAc化があらゆる心肥大の共通基盤であることを解明しました(iScience. 2021)。心筋リモデリングにおけるCa代謝異常(Sci Rep. 2019, Nat Commun. 2023)、オルガネラ異常(Commun Biol. 202)の新たな制御機構も明らかにしました。現在、ミトコンドリア以外のオルガネラの心筋リモデリングの役割および細胞連関・臓器連関について解明を進めています。細胞機能は最終的にタンパク機能に依存するため、タンパク翻訳後修飾についても研究を行っています。
心血管疾患におけるフェロトーシスを基軸とした病態解明と治療法の開発
新たに提唱された「鉄依存性の細胞死フェロトーシス」を基軸として心血管疾患の病態解明と治療法の開発に取り組んでいます。これまでにアントラサイクリン心毒性の発症においてフェロトーシスが重要な役割を果たしていること(JCI Insight, 2020)、この機序としてヘム合成異常によるミトコンドリア内の鉄過剰が原因となっていることを明らかにしてきました(Science Signal, 2022)。これらの病態解明に基づき、5-アミノレブリン酸の投与がヘム合成を促進し、鉄過剰とフェロトーシス、ひいてはアントラサイクリン心筋症の発症を予防できることを示してきました。本研究成果に基づき、5-ALAによるアントラサイクリン心毒性の抑制薬の臨床開発にも取り組んでいます。
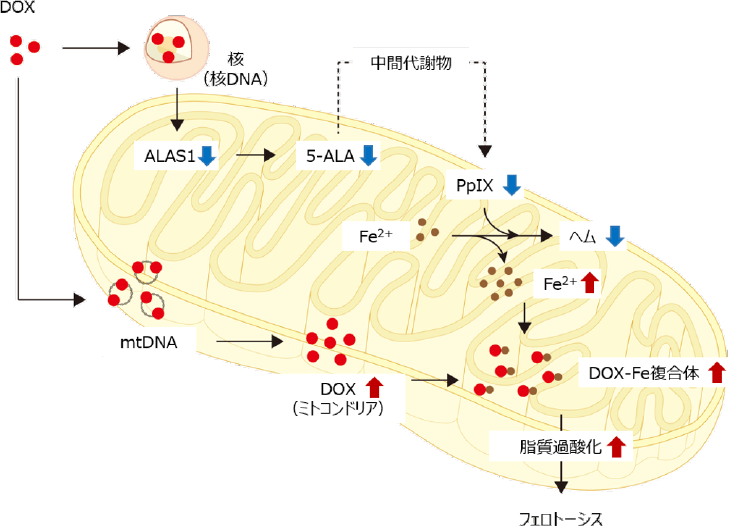
(258): eabn8017 (2022)
また、虚血再灌流傷害においてもフェロトーシスが重要な役割を果たしていることを明らかにしてきました。虚血再灌流傷害においてはヘムオキシゲナーゼ-1の発現が亢進することにより、小胞体内に鉄過剰が生じることがフェロトーシスの誘因であることを明らかにし、フェロトーシスの抑制が遠隔期の心機能維持を可能とする治療戦略になることを明らかにしました(JACC Basic Transl Sci, 2022)。本成果に基づき、鉄のキレート剤であるデフェラシロクスが心筋梗塞時の虚血再灌流傷害に対する新たな治療法になることを示し、現在臨床研究開発に取り組んでいます(J Am Heart Assoc, 2024)。
心不全における慢性炎症を基軸とした病態解明と治療法の開発
心不全の病態進展において慢性炎症が深く関与していることが多くの研究により明らかにされてきました。私たちは、心不全の慢性炎症の制御にNKT細胞の活性化が有効な治療法となり得ることを示し、臨床研究開発に取り組んできました(CircHF, 2022)。また、慢性炎症の原因となっている病態として、抗心筋自己抗体に着目し、世界で初めて抗心筋自己抗体を生じる心不全動物モデルの確立に成功し、同モデルの解析を進めてきました(CircHF, 2023)。本モデルの解析を通じ、ラパマイシンが自己抗体の生成を抑制することを明らかにしています。本研究は、心不全における骨格筋機能不全に関する研究へと発展しており、「抗心筋自己抗体を介した心臓-骨格筋連関」という新たな病態概念の構築に向けて取り組んでいます。
心血管疾患における低酸素応答の役割解明と治療応用に関する研究
心血管疾患において虚血(低酸素)は極めて重要なトピックであり、盛んに研究が取り組まれてきました。しかしながら、虚血に対する低酸素応答は複雑に病態に関与しているため、心血管疾患におけるその理解は未だ十分とはいえません。私たちは、低酸素応答の主たる制御分子であるHIF-1αに着目し、HIF-1αが病態に応じて二面性を持つことを前提に研究を進めています。これまで、HIF-1αによる適応反応を薬理学的に誘導することで、急性の虚血に対する耐性を示し、保護的に作用することを明らかにしてきました(CircJ, 2020)。一方で、心筋梗塞などの極度の虚血の場合には、低酸素応答の過応答により心筋細胞死を誘導し、心筋梗塞時の心破裂の発症に関与していることを明らかにしてきました(J Am Heart Assoc, 2021)。現在、心筋の収縮不全にもHIF-1αの過応答が関与していること、そしてそのメカニズムの解明に取り組んでいます(Nature Cardiovasc Research, under revision)。

HFpEFにおけるPDE1Aの病態機能解明に関する研究
ヒトや動物モデルの解析から得られたデータを基に、HFpEFにおいては小胞体ストレス誘導性のカルシウム動態異常(ストア作動性カルシウム流入)を介したphosphodiesterase 1A(PDE1A)の活性化が病態進展に重要な役割を担っていることを明らかにしました。HFpEF新規治療法開発につながる重要な標的と考えています。
右心不全の病態進展におけるPDE10AおよびSIK3の役割の解明
右心不全は未だに治療法が確立されておらず、心不全におけるさまざまな薬物療法・非薬物療法の進歩の中でLVAD後の右心不全も未解決の重要な問題です。動物モデルを用いて、phosphodiesterase 10A(PDE10A)やsalt-inducible kinases(SIKs)が右心不全の病態進展において果たしている重要な機能をを明らかにする研究を行っています。
